清华&智源研究成果登《Science》:DrugCLIP用AI驱动百万倍速药物筛选,开启全基因组靶向时代
在计算生物学领域,有一个被追逐了数十年的“圣杯”——化学基因组学。其核心愿景是实现对全基因组蛋白质靶点的全覆盖,为每一个潜在的生命密码配上一把精准的“药物钥匙”。人类基因组编码约 20000 种蛋白质,其中 90% 与疾病密切相关,却长期处于 “无药可靶” 状态。面对如此庞大的潜在靶点空间与近乎无限的小分子化学库,传统药物筛选方法如同大海捞针,即使依靠当前最先进的分对接工具,完成全基因组规模的筛选也需数百年,严重制约了突破性疗法的发现。
1月9日,清华大学智能产业研究院(AIR)- 北京智源人工智能研究院“健康计算联合研究中心” 兰艳艳教授课题组的主导下,研发的AI 驱动的超高通量药物虚拟筛选平台 DrugCLIP,在顶刊《Science》重磅发表。DrugCLIP不仅实现了药物筛选速度的百万倍级提升,更首次完成了全基因组规模的药物映射,将化学基因组学的宏伟梦想照进现实。兰艳艳系清华大学智能产业研究院(AIR)教授,智源学者,青源会发起成员。
范式重构:从“物理模拟”到“跨模态向量检索”的技术跃升
传统药物筛选长期受困于“不可能三角”:精度、通量与化学空间规模。传统的分子对接高度依赖原子级的物理受力模拟,面对万亿级分子库时,庞大的计算代价让全基因组筛选成了不可能完成的任务。
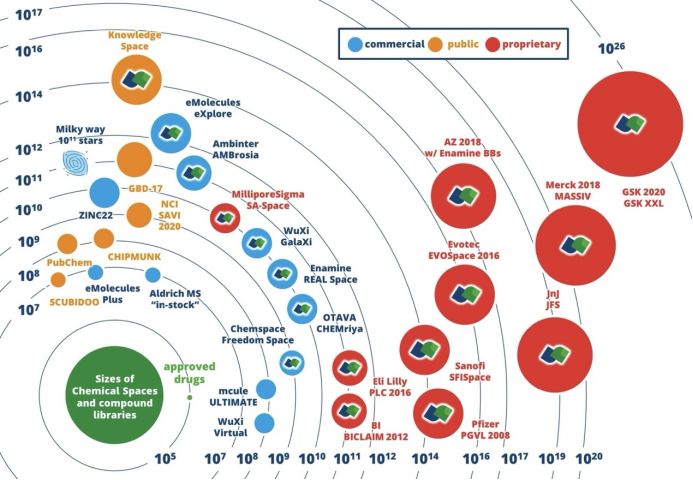
DrugCLIP 的核心创新在于创造性地构建了蛋白质口袋与小分子的“向量化结合空间”。它不再执着于模拟分子如何“卡入”蛋白的动态过程,而是利用深度对比学习技术,将复杂的生物相互作用重构为计算机领域极度成熟的向量检索问题。
在这种硬核架构下,团队展现了极具前瞻性的 AI 逻辑:
- 自监督结构预训练: 团队创造性地从海量蛋白数据中切取片段模拟“假配体”,构造了多达 550 万组 训练样本。这种策略让 AI 在接触真实药物前,就已深刻领悟了蛋白表面的结构特征,赋予了模型极强的 Zero-shot泛化能力。
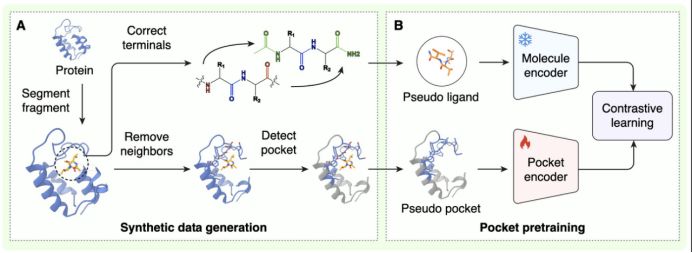
- 多尺度表征对齐: 团队通过训练两个深度神经网络编码器,将蛋白口袋的 3D 拓扑结构与小分子的化学表征映射到同一个高维共嵌入空间(Joint Embedding Space)。
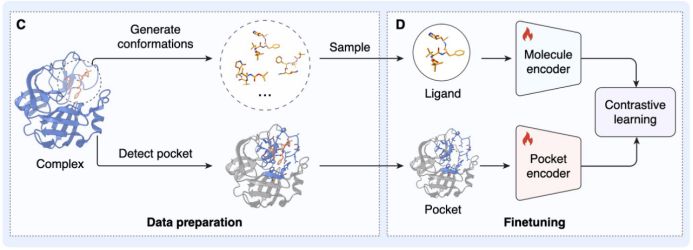
这种算法级的范式转换,直接将单节点(128核 CPU + 8张 GPU)的日打分能力推向了 10 万亿次(10的13次方) 的巅峰。相较于传统工具,筛选效率提升了 100 万倍。
从预测到验证:攻克“暗靶点”与 AlphaFold 结构的无缝对接
DrugCLIP 的价值不仅在于算力的飞跃,更在于其对全新靶点的硬核筛选能力。针对此前既无实验结构、也无已知抑制剂的“暗靶点”——人源 E3 泛素连接酶 TRIP12(与癌症和帕金森相关),DrugCLIP 直接基于 AlphaFold2 预测的蛋白结构进行盲筛,成功命中多个活性抑制剂。
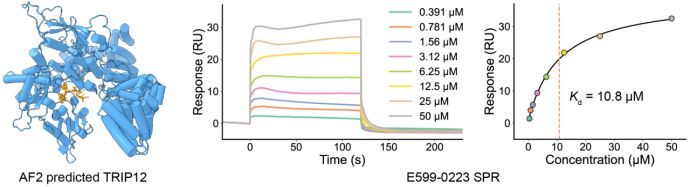
在临床靶点 NET(去甲肾上腺素转运体)的实验中,DrugCLIP 筛选出的候选分子中有 15% 证实有效,且部分分子的活性直接超越了现有的一线临床药物。相关复合物结构已通过冷冻电镜解析,进一步验证了其生物学可信度。
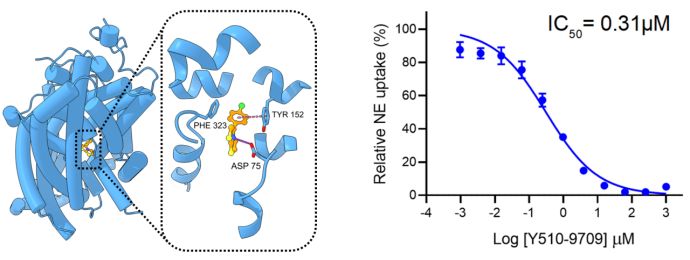
赋能万众创新:开启基因组级药物发现生态
为了践行赋能科研社区、重塑药物研发现状的愿景,研究团队利用 DrugCLIP 完成了人类历史上首次全基因组规模的虚拟筛选:覆盖约 1 万个蛋白靶点、2 万个结合口袋,对超过 5 亿个小分子进行全量对齐,产出 200 万个高潜力靶点分子对,并据此构建了目前全球规模最大的蛋白-配体筛选数据库GenomeScreenDB。
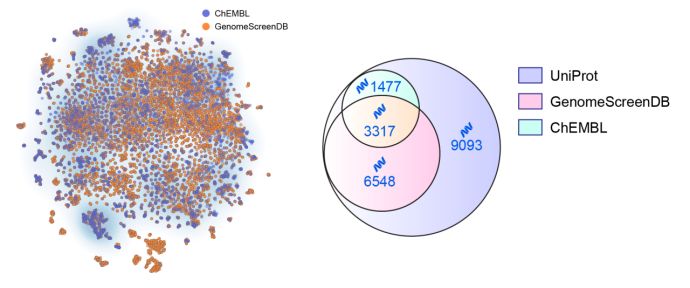
早在 2025 年 6 月,清华 AIR 已联合智源研究院预先发布了 DrugCLIP 平台,正式向全球科研社区免费开放。截至目前,该平台已吸引了超过千余名科研人员深度使用,累计完成了超过万次大规模筛选任务。 这种极速、低门槛的筛选体验,正在极大地降低新靶点开发的起始门槛。
针对这一划时代的成果与平台的开放,北京生命科学研究所所长、中国科学院院士王晓东评价道:
“DrugCLIP 大大提高药物发现的速度,不仅仅是时效的提升,更大的作用是扩展候选化合物的空间,降低了制药的门槛,为万众创新提供了可能,为新药研发创造更好的生态环境。AI 药物研发更有意义的应用场景是发现新的可药靶点。”
DrugCLIP在《Science》的发表,不仅是对技术突破的国际认可,更意味着药物研发正式迈入“后AlphaFold时代”的规模化、系统化新阶段。从孤立靶点攻关到全景化探索,从封闭研发到开放协作,DrugCLIP作为AI4S(AI for Science)重塑生命科学底层逻辑的绝佳范例,正在重新定义药物发现的路径与边界,推动人工智能成为下一代医疗突破的核心驱动力。
论文地址:https://www.science.org/doi/10.1126/science.ads9530
DrugCLIP 平台地址: https://www.drugclip.com
DrugCLIP 实现了从“大海捞针”到“精准定位”的筛选突破,在速度与规模上取得了重大进展。在此基础之上,进一步提升靶点与药物分子匹配的精度、推动药物从筛选到设计的全链条贯通,成为接下来的关键方向。
承接这一方向,北京智源人工智能研究院自主研发了全原子微观生命模型OpenComplex2,旨在药物筛选的精度和机理层面做进一步的深化探索。OpenComplex2实现了药物筛选从静态结构预测走向动态构象全景建模,通过预测自由能景观的方式,清晰描绘靶点与药物分子间的动态作用的全貌,为候选分子的微观机理验证与结构优化提供理论依据,有望加速从基础分子机制研究向临床药物设计的转化。
未来,DrugCLIP的广度筛选与OpenComplex2的深度模拟将形成合力,与科研产业生态合作伙伴深度协同,共同推进在肿瘤、感染性疾病、罕见病等领域的新靶点与First-in-class药物的发现,助力构建更智能、高效、普惠的全球药物创新生态。
本文由方向对了资讯网发布,不代表方向对了资讯网立场,转载联系作者并注明出处:https://www.zhenyes.com/industry/6574.html

